Hoy en día, el único tratamiento posible para la enfermedad celíaca es seguir de por vida una dieta sin gluten, algo no siempre sencillo porque se trata de una proteína muy usada en la industria alimentaria. Pero dos hallazgos en los últimos años hacen un poco más probable el que algún día los celíacos puedan comer normalmente. Uno se basa en el estudio de las causas íntimas de la enfermedad; el otro, en una enzima capaz de desmenuzar el gluten y volverlo inofensivo. Los investigadores afirman que las perspectivas son buenas.
 Imagen: Jean Scheijen
Imagen: Jean Scheijen
La enfermedad celíaca afecta en Europa a una de cada 150 personas, lo que la convierte en la enfermedad crónica intestinal más frecuente en España; tiene base genética y a menudo no está diagnosticada, dado que a veces cursa sin síntomas o éstos, que son muy variados, se confunden con los de otras enfermedades; los más frecuentes son pérdida del apetito y de peso, diarrea crónica, distensión abdominal, alteraciones del carácter y retraso del crecimiento.
Está producida por una intolerancia permanente al gluten, una proteína que se encuentra en el trigo, la cebada, el centeno, la espelta, el kamut, el triticale y posiblemente en la avena. Esta intolerancia da lugar a una atrofia de las vellosidades del intestino, lo que a su vez, impide la absorción normal de los nutrientes (proteínas, grasas, hidratos de carbono, sales minerales y vitaminas).
Enfermedad autoinmune
Se sabe también que es una enfermedad de tipo autoinmune: por alguna razón el organismo de los celíacos reacciona al gluten creando anticuerpos que atacan el propio intestino, y que pueden dañarlo de forma grave. Además, es frecuente que los celíacos padezcan también otras enfermedades de este tipo. Pero, ¿cuáles son sus causas últimas? ¿Qué genes intervienen? A pesar de su alta incidencia, sigue siendo una enfermedad bastante poco conocida.
Como explica Frits Koning, investigador de la Universidad de Leiden (Países Bajos), «es una enfermedad con un amplio espectro de síntomas. No todos los pacientes están igual de afectados y no sabemos por qué. Se sabe que está asociada con un gen, el HLA-DQ2, pero el 25% de los caucásicos lo tenemos y sin embargo sólo alrededor de uno de cada cien sufre la enfermedad. Así que en muchos sentidos es una enfermedad desconcertante».
El único tratamiento eficaz por ahora es eliminar el gluten de la dieta. «Parece fácil, pero especialmente el gluten está muy presente en las dietas occidentales», prosigue Koning. El gluten se usa a menudo como aditivo alimentario, porque es una forma barata de aumentar el contenido proteico y da elasticidad a la masa. Por ejemplo, «los celiacos pueden comer patatas fritas de bolsa, pero no si llevan pimentón u otras especies, porque estos aditivos se adhieren a las patatas mediante gluten», explica Koning.
La puerta al sistema inmunitario
La intolerancia al gluten da lugar a una atrofia de las vellosidades del intestino que impide la absorción normal de los nutrientes
Hace seis años los investigadores empezaron a arrojar algo de luz sobre las causas de la intolerancia al gluten. Un grupo de la Universidad de Maryland, EEUU, publicó en la revista médica The Lancet el hallazgo de que los celíacos tienen niveles especialmente altos de la proteína zonulina, que regula la permeabilidad del intestino, durante las fases agudas de la enfermedad.
«La zonulina funciona como el guardia de tráfico o el portero de los tejidos corporales», explicaba entonces Alessio Fasano, catedrático de pediatría y fisiología de la Universidad de Maryland. «Y nuestro portal de entrada principal es el intestino, con sus miles de millones de células. La zonulina ensancha el espacio entre las células, permitiendo que entren algunas sustancias pero dejando fuera bacterias dañinas y otras toxinas», añadía el experto.
«En la enfermedad celíaca no entendíamos cómo una proteína tan grande como el gluten lograba atravesar la barrera. Y ahora ya tenemos la respuesta», explica Fasano. Según este experto, los altos niveles de zonulina presentes en los celíacos hacen que «las puertas se mantengan abiertas de par en par, permitiendo la entrada al gluten y otros alergenos». Una vez que estos compuestos quedan expuestos al sistema inmune, los anticuerpos los atacan (y al propio intestino).
Tras ese hallazgo, el paso lógico por parte de las empresas farmacéuticas era buscar una manera de inhibir o bloquear la zonulina. La compañía Alba Therapeutics anunció el pasado 21 de septiembre que su fármaco AT-1001, un inhibidor de la zonulina que se administra por vía oral para el tratamiento de la enfermedad celíaca, entraba en ensayos de fase II, en los que se estudiará la seguridad, grado de tolerancia y eficacia del fármaco en 79 afectados. Hace un año, la Agencia del Medicamento Estadounidense (FDA) asignó a este fármaco la categoría de ?fast track?, fármaco contra enfermedades sin tratamiento en el mercado.
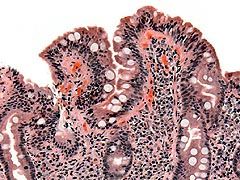 Imagen: Wikipedia
Imagen: Wikipedia
Otra novedad en relación a un posible tratamiento oral contra la enfermedad celíaca se dio a conocer el pasado junio. El grupo de Koning ha hallado una enzima, laprolyl endoproteasa (PEP), investigada originalmente para el procesado comercial de alimentos y presente en el hongo Aspergillus Níger (AN). «A la luz de nuestros resultados, ahora hay una posibilidad real de desarrollar un suplemento oral con una enzima capaz de degradar el gluten en el estómago, antes de que llegue al intestino delgado, donde causa problemas a los celíacos», ha declarado Koning, cuyo trabajo se ha publicado en la revista American Journal of Physiology- Gastrointestinal and Liver Physiology, de la Sociedad Americana de Fisiología.
La idea de buscar una manera de degradar el gluten artificialmente fue propuesta inicialmente ya en los años cincuenta. Y el propio grupo de Koning había hallado previamente otra enzima capaz de ?hacer el trabajo?, pero con el inconveniente de que se inactivaba en las condiciones ácidas del estómago. También era importante su ?rapidez?, porque en el estómago, que es donde el gluten debe ser degradado para evitar su llegada al intestino, la comida permanece un tiempo limitado, entre una y cuatro horas. Los investigadores han demostrado ahora que la nueva enzima, llamada AN-PEP, trabaja perfectamente en los medios muy ácidos, y que es sesenta veces más rápida que la enzima hallada previamente por el grupo. AN-PEP «despedaza el gluten en fragmentos inocuos», explican los investigadores. Además, «es muy estable y puede ser fabricada a un coste aceptable en un entorno industrial», añaden.
Como en el caso de los inhibidores de la zonulina, los investigadores ya han anunciado que esperan poder iniciar en un futuro los ensayos clínicos en humanos dado que no hay un modelo animal para la enfermedad celíaca. No dieron, sin embargo, una fecha. Fasano explica que «es sin duda previsible que haya en el futuro alternativas terapéuticas a la dieta sin gluten». Así permiten predecirlo el conocimiento científico, las técnicas disponibles actualmente y los grandes progresos realizados en comprensión de las bases de la enfermedad celíaca. «Lo que no es predecible es el tiempo que nos llevará [desarrollar estos tratamientos]». En su opinión, «la nueva enzima capaz de degradar gluten es mucho más prometedora que las halladas previamente», aunque considera que el trabajo con la zonulina está más adelantado.






